问题
-
某微溶化合物AB2C3的饱和溶液的离解平衡为:。今测得A的浓度为1.00×10-3mol·L-1,问AB2C3的Ksp为多少?
-
已知H2SO4的=1.0×10-2,求PbSO4沉淀在0.10mol·L-1的HNO3中的溶解度。(Ksp=1.6×10-8)
-
微溶化合物A2B3在溶液中的电离平衡是:,今已测得B的浓度为3×10-3mol·L-1,则该微溶化合物的溶度积Ksp是______
-
浓度为25.5μg/50mL的Cu2+溶液,用双环乙酮草酰二腙光度法进行测定,于波长600nm处用2cm吸收池进行测量,测得T=
-
由某挥发油中分出一种纯物质,在己烷中测得λmax=242nm,其他分析方法初步确定该化合物的结构可能为如下(A)或(
-
分别向沉淀物PbSO4(Ksp=1.6×10-8)和PbCO3(Ksp=7.4×10-14)中加入

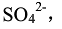 ,产生PbSO4沉淀,并调至
,产生PbSO4沉淀,并调至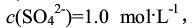 。实验测得电动势E=0.62V(已知铜为正极),计算PbSO4的Ksp。
。实验测得电动势E=0.62V(已知铜为正极),计算PbSO4的Ksp。 冀公网安备 13070302000102号
冀公网安备 13070302000102号